Polluants
O3 – Ozone
L'ozone (O3) est un constituant mineur de l'atmosphère pour lequel l'intérêt de la communauté scientifique s'est accru ces dernières années pour deux raisons :
- Des diminutions importantes de la teneur en ozone de la stratosphère (qui représentent normalement 90% de l'ozone total), ont été observées en certaines circonstances. Ces diminutions sont susceptibles de conséquences néfastes pour la vie sur Terre car ce "bon" ozone joue le rôle d'écran protecteur pour les êtres vivants en absorbant une partie du rayonnement ultraviolet nocif pour la santé.
- Une production excessive d'ozone dans les grands centres urbains et industriels, qui est à l'origine d'une pollution de la troposphère lors de conditions météorologiques particulières (épisodes estivaux de pollution). Ce "mauvais" ozone est toxique pour la santé humaine et la végétation au-delà d’un certain seuil d’exposition.
L'ozone stratosphérique est produit à partir de la recombinaison entre un atome d’oxygène O produit par photolyse d’une molécule de dioxygène (O2) et d’une autre molécule de dioxygène. Le même mécanisme existe dans la troposphère où la photolyse de NO2 est alors la source de l’atome oxygène. La production d'ozone troposphérique est donc majoritairement localisée au voisinage des sources de NO2, c’est à dire les grands centres urbains et industriels, et les zones de combustion de biomasse. L’ozone ainsi produit est détruit assez efficacement par photolyse* dans le proche UV et le visible, et par dépôt au sol.
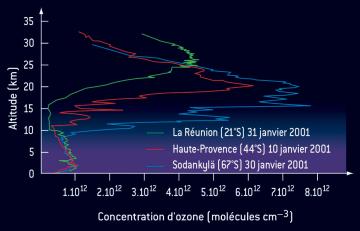
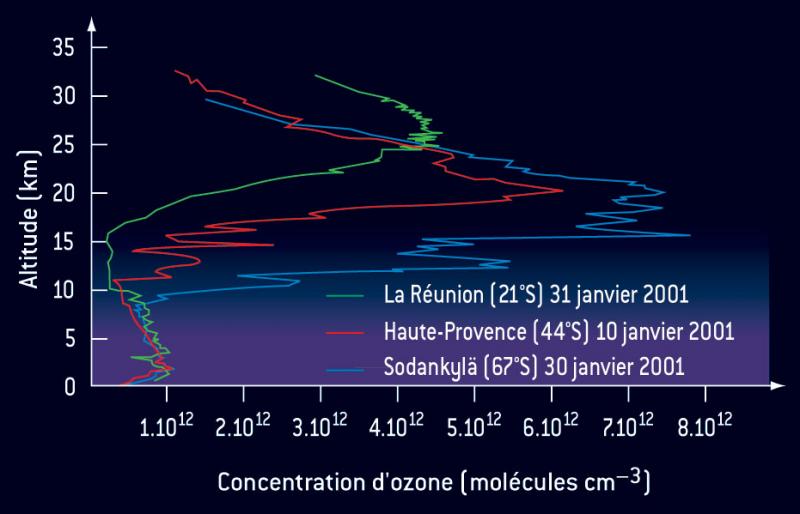
La concentration d’ozone est faible dans la troposphère, augmente brusquement à partir de la limite entre troposphère et stratosphère (tropopause) pour atteindre un maximum dans la basse stratosphère, situé entre 15 et 20 km au niveau du pôle d’hiver, et entre 25 et 30 km à l’équateur (cf. figure). Au-dessus de 30 km, la concentration d’ozone décroît très rapidement.
La circulation moyenne le long des méridiens de la Terre transporte l’ozone depuis les régions équatoriales vers le pôle d’hiver en s'accompagnant d’un lent mouvement vers le bas: c’est pourquoi l’altitude du maximum de concentration d’ozone décroît à mesure qu’on approche des régions polaires
I Introduction
L'ozone ou tri-oxygène (O3) est un constituant mineur de l'atmosphère, à l'égard duquel l'intérêt porté par la communauté scientifique s'est accru au cours de ces dernières années pour plusieurs raisons :
- Les diminutions importantes de la teneur en ozone de la stratosphère, observables en certaines circonstances, sont susceptibles de conséquences néfastes pour la vie sur Terre car l'ozone joue le rôle d'un écran protecteur pour les êtres vivants en absorbant les rayonnements ultraviolets de plus courtes longueurs d'onde.
- La production excessive d'ozone dans les grands centres urbains et industriels est à l'origine d'une pollution de latroposphère lors de conditions météorologiques particulières.
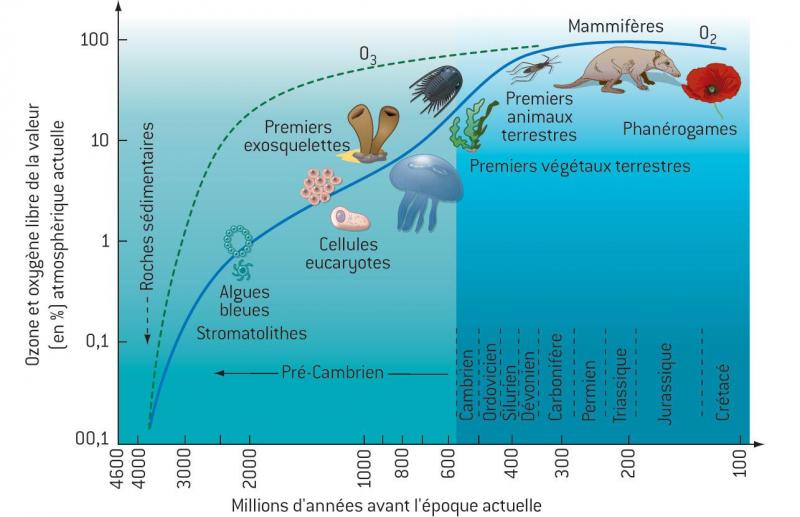
On a coutume de dire qu’il existe deux types d'ozone. Un "bon" ozone, l’ozone stratosphérique, qui grâce à son rôle protecteur vis-à-vis du rayonnement UV, a permis à la vie biologique de se développer hors de océans (voir figure 1), et un "mauvais" ozone, produit près de la surface par réactions photochimiques impliquant des polluants d’origine humaine, notamment les oxydes d’azote. L’ozone est alors un polluant toxique pour la santé humaine et la végétation au-delà d’un certain seuil d’exposition.
L’apparition de l’oxygène est le phénomène déterminant qui a permis l’évolution de la biosphère en initiant de nouveaux processus biochimiques aérobies. Par ailleurs, la photolyse de O2 dans la stratosphère a induit la formation de la couche d’ozone qui atteint des concentrations proches des valeurs actuelles il y a 400 Ma (cf. figure 1). Grâce à sa capacité d’absorption du rayonnement UV, l’ozone a considérablement réduit le flux UV à la surface de la Terre, permettant ainsi le développement d’organismes multicellulaires. Les premiers organismes multicellulaires trouvés dans les sédiments océaniques datent de - 680 Ma.
Dans la stratosphère, l’ozone est produit à partir de la recombinaison entre un atome d’oxygène, produit par photolyse* d’une molécule d’oxygène (O2) à des longueurs d'onde de 250nm, et d’une autre molécule d’oxygène. Le même mécanisme existe dans la troposphère où la photodissociation de NO2 dans le visible à des longueurs d'onde supérieures à 400 nm est alors la source de l’atome oxygène car le rayonnement UV < 250 nm ne pénètre pas dans la troposphère. Cette production sera donc majoritairement localisée au voisinage des sources d’oxydes d’azote, c’est à dire les grands centres urbains, industriels, ou les zones fréquemment perturbées par les processus de combustion de la biomasse. L’ozone ainsi produit est détruit assez efficacement par photodissociation dans le proche UV et le visible et par déposition au sol. Les concentrations d’ozone exprimées en rapport de mélange sont ainsi beaucoup plus faibles dans la troposphère (rO3 <100 ppb) que dans la stratosphère (rO3<1 ppm).
II Ozone stratosphérique
Lorsque que l’on observe globalement l’ozone atmosphérique sa répartition est largement dominée par celle de l’ozone stratosphérique qui représente plus de 90% de l’ozone total.
II-1 Répartition horizontale de l’ozone stratosphérique
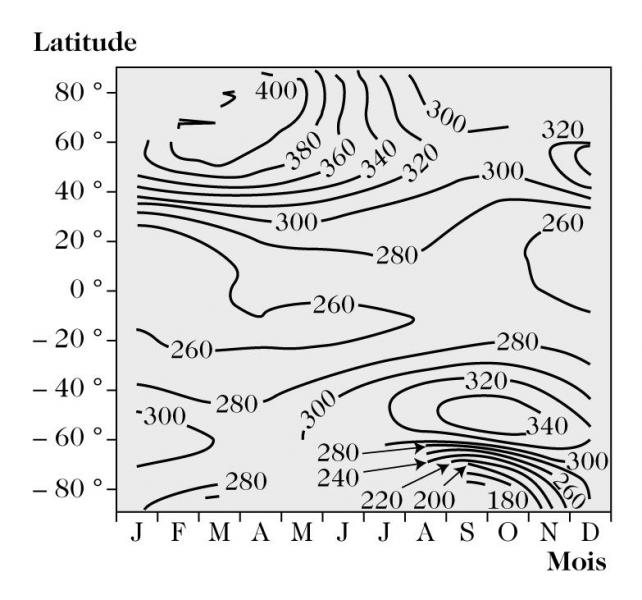
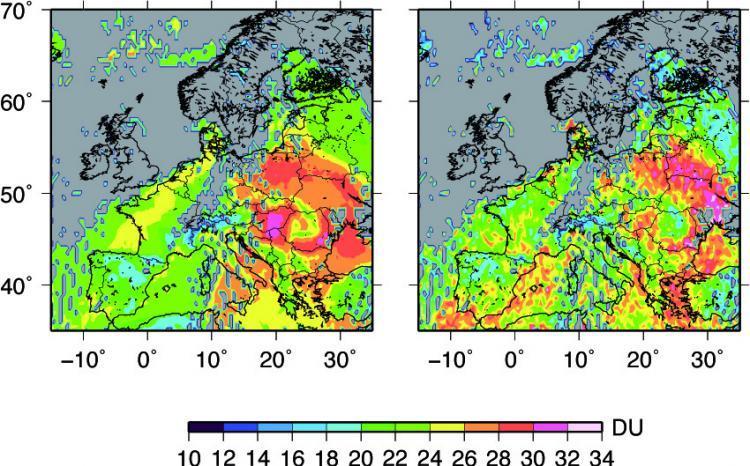
L’efficacité de l’absorption du rayonnement solaire ultraviolet (longueur d'onde de 240 à 320 nm) au cours de sa traversée de l’atmosphère dépend de l’épaisseur locale de la couche d’ozone, c’est-à-dire du nombre total de molécules d’ozone le long du trajet optique des rayons. Cette épaisseur est appelée colonne totale d’ozone, car elle représente la quantité totale d’ozone contenue dans une colonne d’air s’étendant de la surface jusqu’au sommet de l’atmosphère. Elle est le plus souvent exprimée en unité Dobson (symbole DU). Une unité Dobson correspond à une épaisseur théorique d’ozone d’un centième de millimètre à température et pression standard (273 K et 1 atmosphère). Elle représente 2,69 x 1016 molécules d’ozone par cm². La valeur moyenne globale de la colonne d’ozone moyennée sur l’année est de l’ordre de 300 DU, soit 3 mm d’épaisseur théorique. L’ozone est principalement produit dans les régions équatoriales où le rayonnement solaire est suffisamment intense pour photolyser constamment l’oxygène moléculaire. Or, paradoxalement, la colonne totale d’ozone est maximale près des pôles, loin de sa région de production (figure 2). De plus, la colonne totale des hautes et moyennes latitudes n’est pas corrélée à la quantité de lumière disponible, puisqu’elle atteint son maximum pendant l’hiver et le printemps au lieu de l’été, et son minimum en automne au lieu de l’hiver. Il est donc clair que la distribution spatiale et temporelle de l’ozone dans la stratosphère n’est pas simplement déterminée par l’équilibre photochimique entre sa production et sa destruction. Les mouvements dynamiques associés aux vents et à la circulation générale jouent en effet un rôle fondamental en redistribuant l’ozone à travers l’ensemble de la stratosphère.
II-2 Répartition verticale de l’ozone stratosphérique
La concentration d’ozone est faible dans la troposphère, augmente brusquement à partir de la tropopause pour atteindre un maximum dans la basse stratosphère, situé entre 15 et 20 km au niveau du pôle d’hiver, et entre 25 et 30 km à l’équateur (figure 3). Au-dessus de 30 km, la concentration d’ozone décroit exponentiellement. Le rapport de mélange d’ozone atteint une valeur d’environ 10 ppmv à l’équateur vers 35 km. Comme le suggère la répartition en latitude de la colonne d’ozone, l’examen de la distribution verticale de l’ozone stratosphérique révèle des concentrations maximales aux hautes latitudes en hiver, et non dans sa région de production, à l’équateur. Cela illustre a nouveau l’importance de la circulation méridienne moyenne qui transporte l’ozone depuis les régions équatoriales vers le pôle d’hiver. Ce transport horizontal s’accompagne d’un lent mouvement de subsidence : c’est pourquoi l’altitude du maximum de concentration d’ozone décroit à mesure qu’on approche des régions polaires (figure 3).
III Ozone troposphérique
III-1 Origine de l’ozone troposphérique
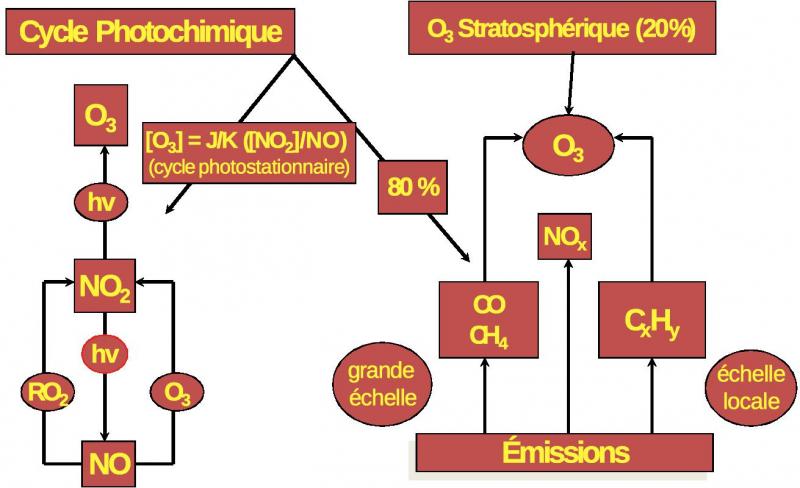
Dans la troposphère, la principale cause de formation de l’ozone est la photolyse du dioxyde d’azote (NO2) par le rayonnement solaire à une longueur d’onde inférieure à 420 nm. L’efficacité de cette réaction est caractérisée par le taux de photolyse J qui est fonction de l’ensoleillement. Elle conduit au monoxyde d’azote (NO) et à l’oxygène monoatomique (O). Ce dernier en réagissant avec le dioxygène donne de l’ozone.
NO2 + hν -> NO + O (1) M est une molécule catalyseur de la réaction (généralement N2 ou O2)
O + O2+ M -> O3 + M (2)
En fait l’ozone peut aussi réagir avec le monoxyde d’azote présent pour redonner du NO2 :
NO + O3 -> NO2 + O2 (3).
La constante cinétique (vitesse) de la réaction 3 est notée K. En première approximation, le taux de production d’ozone dépend du rapport des concentrations des oxydes d’azote dans l’atmosphère :
[O3] = K/J (NO2/NO).
Ceci correspond à un état dit photostationnaire, contrôlé notamment par la valeur du taux de photolyse J, qui varie avec l’ensoleillement. Sur un cycle journalier moyen, le cycle photostationnaire des oxydes d’azote n’aboutirait pas à une production nette d’ozone significative. Dans une atmosphère polluée cependant, l’oxydation, notamment par le radical OH, d’autres composés (les hydrocarbures, mais aussi le méthane et le monoxyde carbone), conduit à la formation d’espèces radicalaires telles que les radicaux péroxyles (HO2) ou organiques (par exemple méthyl-péroxyde CH3O2). Ces radicaux ont une capacité d’oxydation des molécules de NO en NO2 supérieure à celle de l’ozone, de sorte que l’équilibre photostationnaire est déplacé dans le sens d’une production nette d’ozone (le rapport NO2/NO augmente). En effet le NO2 est alors reformé sans qu’il y ait destruction d’ozone. On estime qu'environ 80% de l’ozone de la troposphère résulte d’une formation photochimique dans les basses couches. Seulement 20% a une origine stratosphérique (figure 4). Dans cette formation photochimique, on distingue la formation à l’échelle locale, qui est due à la production de radicaux péroxyles par oxydation des hydrocarbures (dans les panaches de pollution des villes par exemple), d’une formation à grande échelle plutôt causée par l’oxydation du méthane et du monoxyde de carbone. Ceci est lié au fait que les vitesses d’oxydation et donc les durées de vie des hydrocarbures dans l’atmosphère (quelques heures à quelques jours) sont beaucoup plus faibles que celle du CO (2 mois) ou du méthane (10 ans).
La formation photochimique d’ozone, qui cause notamment les épisodes de pollution, est un phénomène relativement complexe. Cette formation dépend de façon non linéaire de plusieurs gaz précurseurs, notamment les composés organiques volatils (COV) et les oxydes d’azote (NOx), et de l’ensoleillement. Dans l’atmosphère urbaine par exemple, l’ozone est en général en moyenne détruit en raison d’un excès d’oxydes d’azote. La formation importante intervient plutôt en zone rurale dans le panache urbain, après dilution des oxydes d’azote. Dans ce panache, le taux de formation d’ozone est plus ou moins important selon les valeurs relatives des concentrations des précurseurs. L’efficacité de formation d’ozone est en fait contrôlée par la valeur du rapport NOx/COV.
Le transport d’ozone de la stratosphère dans la troposphère est principalement dû à des processus de déformation de la tropopause qui ont pour origine la formation de zones frontales en altitude au voisinage des courants jet qui dominent la circulation d’ouest des masses d’air dans les subtropiques
(latitude de 30°), et aux moyennes latitudes (latitude de 50°). Ces zones frontales sont inclinées dans un plan vertical et permettent à de l’air stratosphérique, dont l’origine se situe au-dessus de 10-12 km d’altitude, de pénétrer assez profondément dans la troposphère en dessous de 5 km d’altitude. Ces ”langues” d’air stratosphérique sont assez peu larges (<400 km), mais peuvent s’´etaler sur des distances assez grandes (1000 km) le long du courant jet. Ces déformations sont réversibles et une partie de l’air peut retourner vers la stratosphère. Cependant l’étirement de ces fines ”langues” d’air stratosphériques sur de grandes distances permet à l’air stratosphérique riche en ozone de se mélanger à l’air troposphérique par l’intermédiaire de mouvements turbulents à la frontière de cette ”langue”.
III-2 Distribution de l’ozone troposphérique
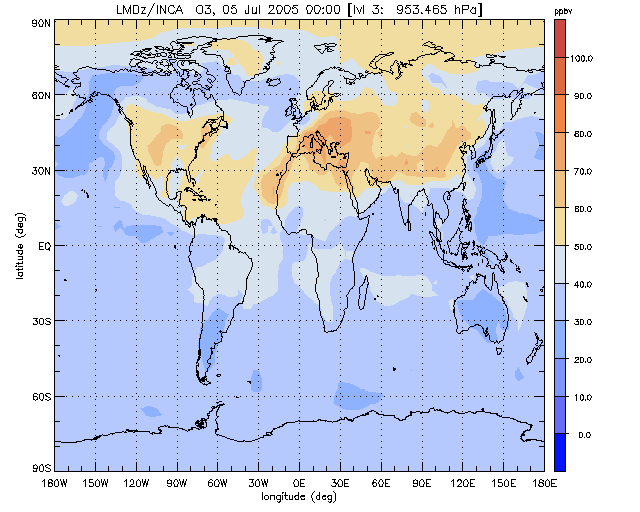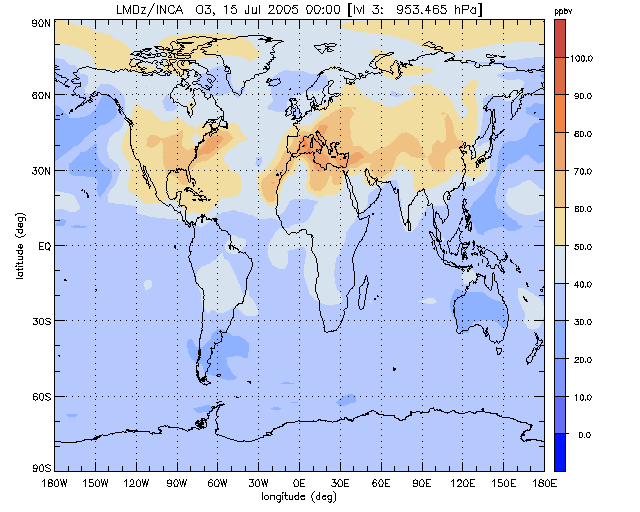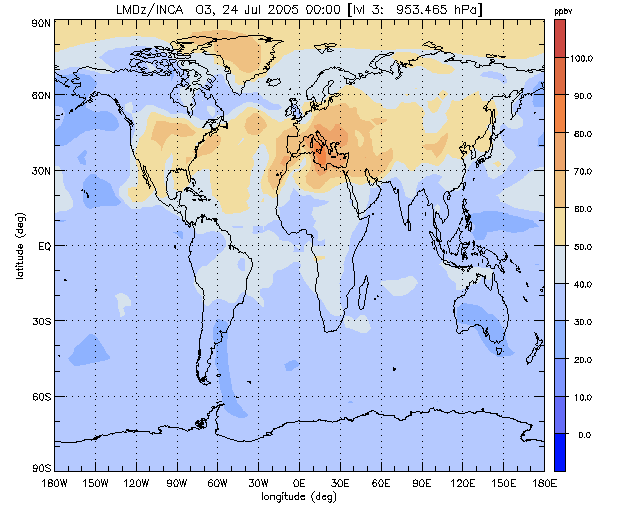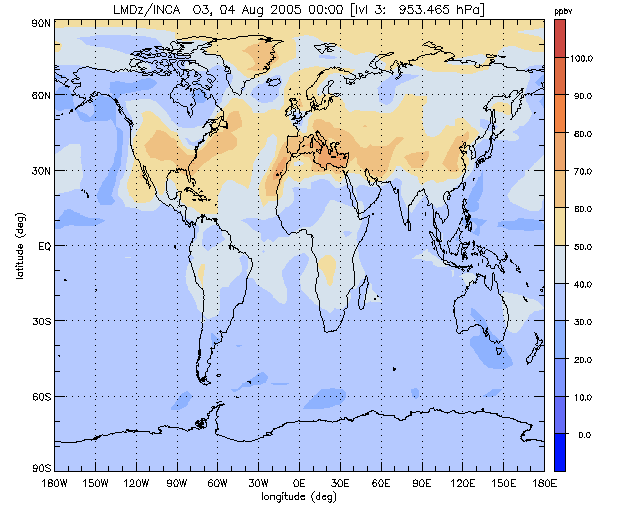
Pour des gaz à longue durée de vie, de l’ordre de la dizaine d’année, comme le CH4 par exemple, les distributions horizontales sont quasi homogènes, avec toutefois une variation méridienne de concentration de l’ordre de quelques pourcents, associée à une plus grande densité des sources dans l’hémisphère Nord. Les gaz, dont la durée de vie, de l’ordre du mois, est inférieure à la durée caractéristique des échanges horizontaux ou verticaux, ont des distributions fortement inhomogènes. C’est de cas de l’ozone troposphérique par exemple, dont un exemple de distribution globale est représenté sur la figure 5. Cette figure montre qu’en été de l’hémisphère Nord, la concentration d’ozone en surface est particulièrement élevée sur les zones continentales où se trouvent l’essentiel des sources de précurseurs photochimiques de l’ozone. Des bulles d’ozone peuvent aussi apparaitre dans la troposphère tropicale, dans les régions affectées par les combustions de biomasse.
Dans la troposphère libre, la concentration d’ozone résulte de processus dynamiques sporadiques transportant l’ozone depuis des régions où il est chimiquement produit, en premier lieu la stratosphère, mais aussi la couche limite continentale polluée. Ces processus dynamiques, fréquents aux moyennes latitudes, ont une variabilité analogue à celle de la formation des dépressions météorologiques. L’analyse de la variation saisonnière des concentrations moyennes mensuelles d’ozone à 500 hPa aux moyennes latitudes révèle un maximum de concentration au printemps, et une amplitude de la variation saisonnière de 20–30 ppb.
Dans la couche limite continentale, on observe une variabilité journalière importante de la concentration d’ozone.L’ozone présente un maximum en milieu de journée, quand la couche limite atmosphérique est bien mélangée et l’activité photochimique à son maximum. Le minimum nocturne s’explique par l’absence de production photochimique, la destruction par réaction chimiques (NO) et par dépôt au sol.
En raison de son importance en chimie atmosphérique, et en tant que polluant pouvant impacter la santé humaine, l’ozone troposphérique est surveillé par un abondant réseau de mesures au sol et de station de radiosondages et de mesures aéroportées. Si l’ozone stratosphérique est depuis longtemps suivi par des observations satellitaires en mesure au limbe (visée tangente) dans l’UV (voir fiche méthodes télédétection spatiales), une nouvelle génération d'instruments satellitaires utilise le domaine infrarouge afin de sonder l'atmosphère par visée au nadir (visée vers le bas), ce qui lui confère un maximum de sensibilité dans la moyenne troposphère. L'instrument IASI (Infrared atmospheric sounding interferometer) développé par le CNES et mis en orbite en octobre 2006 à bord du satellite européen MetOp-A en est un exemple, avec sa couverture spatiale importante, sa fréquence de passage assez élevée (couverture du globe 2 fois par jour), et surtout sa bonne résolution horizontale à basse altitude. Cet instrument, à l’aide de méthodes de traitement adaptées permet la mesure de colonne partielles d’ozone correspondant à la troposphère (Figure 6), ouvrant la voie à un suivi, à terme, de la qualité de l’air dans la basse atmosphère à partir d’observations spatiales?
IV L’ozone : un polluant toxique
L’ozone est un gaz particulièrement important en matière de composition chimique de l’atmosphère par ses impacts multiples. L’ozone stratosphérique est indispensable au maintien de la vie à la surface des continents par le rôle protecteur qu’il joue vis-à-vis du rayonnement UV solaire. Il est au centre de la chimie atmosphérique car il est la source principale du premier oxydant atmosphérique qu’est le radical OH. En revanche, dans les basses couches, la forte concentration l’ozone est aussi un polluant toxique dommageable pour la santé humaine et la végétation. L’ozone pénètre facilement dans les voies respiratoires, sa faible solubilité dans l’eau facilitant son assimilation par les poumons. Ses effets, visibles dès 150 à 200 µg/m3, varient selon la concentration, l’intensité de l’exercice physique et la sensibilité de chacun. L’excès d’ozone provoque toux, inconfort thoracique, gêne douloureuse en cas d’inspiration profonde, essoufflement, irritation des yeux, des voies respiratoires et des poumons, en particulier chez les enfants, les personnes âgées, les asthmatiques et les insuffisants respiratoires. Enfin l’accroissement d’ozone dans la troposphère peut entraîner des nécroses visibles sur les feuilles et les aiguilles d’arbres, mais également sur de nombreux végétaux. Dans les cultures ou les forêts soumises à des niveaux importants d’ozone, on peut observer des pertes de production de plus 10 %, mais cet impact est encore mal quantifié.
Glossaire
Photolyse: on appelle photolyse toute réaction chimique dans laquelle un composé chimique est décomposé par la lumière. Le processus direct est défini comme l'interaction d'un photon et d'une molécule cible. Tout photon avec suffisamment d'énergie peut affecter les liaisons chimiques d'un composé chimique. Ainsi, la photolyse dans l'atmosphère sera le fait de photons du domaine du visible (de 400 à 800nm) et l'ultra violet (de 190 à 400 nm).