Polluants
COV – Composés Organiques Volatils
Les composés organiques volatils non méthaniques (COVNM) sont des espèces gazeuses qui regroupent un grand nombre de composés contenant du carbone et de l’hydrogène (hydrocarbures), voire de l’oxygène dans les cas des hydrocarbures oxygénés. S’ils contiennent d’autres éléments comme du chlore, de l’azote, du fluor, du soufre, ou du phosphore, ils rentrent dans la catégorie générique des COV.
Ils ont de nombreux effets sur la santé. Certains sont toxiques ou cancérigènes (notamment le benzène). En outre, les COVNM, principalement les hydrocarbures, interviennent dans le processus de production d’ozone dans la basse atmosphère. Les COVNM entrent dans la composition des carburants mais aussi de nombreux produits courants contenant des solvants (peintures, colles…). Ils sont émis soit par combustion, soit par évaporation, et dans ces cas, ils contribuent fortement à la pollution urbaine ou industrielle et à la production d’ozone dans les panaches pollués. Néanmoins l’essentiel des émissions des composés organiques volatils est d’origine naturelle, les espèces végétales, dont les arbres, émettant une grande variété de COV.
I Introduction
Les composés organiques volatils non méthaniques (COVNMs) sont des espèces gazeuses qui regroupent un grand nombre de composés contenant du carbone et de l’hydrogène (hydrocarbures), voire de l’oxygène dans les cas des hydrocarbures oxygénés. S’ils contiennent d’autres éléments comme du chlore, de l’azote, du fluor, du soufre, ou du phosphore, ils rentrent dans la catégorie générique des COVs. Ils ont de nombreux effets sur la santé. Certains sont toxiques ou cancérigènes (notamment le benzène). En outre, les COVNMs, principalement les hydrocarbures, interviennent dans le processus de production d’ozone dans la basse atmosphère. Les COVNMs entrent dans la composition des carburants mais aussi de nombreux produits courants contenant des solvants (peintures, colles…). Ils sont émis soit par combustion, soit par évaporation, et dans ces cas, ils contribuent fortement à la pollution urbaine ou industrielle et à la production d’ozone dans les panaches pollués. Néanmoins l’essentiel des émissions des composés organiques volatils est d’origine naturelle, les espèces végétales, dont les arbres, émettant une grande variété de COVs.
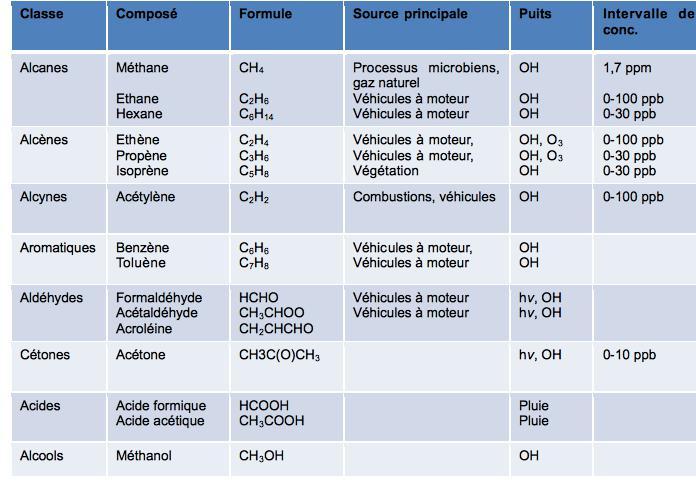
| Classe | Composé | Formule | Source principale | Puits | Gamme de concentration |
| Alcanes | Méthane Ethane Hexane | CH4 C2H6 C6H14 | Processus microbiens, gaz naturel Véhicules à moteur Véhicules à moteur | OH OH OH | 1,7 ppm 0-100 ppb 0-30 ppb |
| Alcènes | Ethène Propène Isoprène | C2H4 C3H6 C5H8 | Véhicules à moteur, Véhicules à moteur, Végétation | OH, O3 OH, O3 OH | 0-100 ppb 0-30 ppb 0-30 ppb |
| Alcynes | Acétylène | C2H2 | Combustions, véhicules | OH | 0-100 ppb |
| Aromatiques | Benzène Toluène | C6H6 C7H8 | Véhicules à moteur, Véhicules à moteur | OH OH | |
| Aldéhydes | Formaldéhyde Acétaldéhyde Acroléine | HCHO CH3CHOO CH2CHCHO | Véhicules à moteur Véhicules à moteur | hv, OH hv, OH | |
| Cétones | Acétone | CH3C(O)CH3 | hv, OH | 0-10 ppb | |
| Acides | Acide formique Acide acétique | HCOOH CH3COOH | Pluie Pluie | ||
| Alcools | Méthanol | CH3OH | OH |
Tableau 1 : Quelques exemples de COVs, les plus importants en chimie atmosphérique (formules chimiques, sources et puits principaux et intervalles de concentration dans l’atmosphère).
II Les différents types de COVs
II.1 Les hydrocarbures non méthaniques (HCNM)
Les hydrocarbures non méthaniques (NMHCs en anglais) sont émis dans l'atmosphère en quantités significatives, à la fois par des sources naturelles et anthropiques. Leur oxydation dans la troposphère a un impact majeur sur la composition chimique de la troposphère. En fonction de la quantité d'oxydes d'azote (NOx) disponibles, l'oxydation des NMHCs dans la troposphère, principalement initiée par réaction avec les radicaux hydroxyles (OH), conduit à la production ou à la destruction chimique d'ozone (O3).
- Alcanes: les carbones ont toutes leurs orbitales de liaisons occupées par un atome d'hydrogène
- Alcènes: présence de double(s) liaison(s)
- Aromatiques: double liaison et structure circulaire
- Alcynes: présence de triple(s) liaison(s)
- Radicaux (notés R): alcanes auquel on a enlevé un atome d'hydrogène (présence d'une paire d'électron libre). Par exemple: radical méthyle CH3., radical éthyle CH3-CH2.
Le méthane est l'hydrocarbure le plus abondant dans l'atmosphère avec 1/3 provenant des sources biogéniques (sols en anaérobiose) et 2/3 anthropiques (gaz naturel, combustions, agriculture, décharge). Il est en général étudié à part dans les processus atmosphériques
Parmi les NMHCs, on observe une grande diversité des concentrations mesurées dans la troposphère. Cette diversité traduit d’abord leur abondance relative au moment de l’émission. Les moteurs diesels émettent par exemple surtout des alcènes, alors que les moteurs essence sont plutôt sources d'alcanes et d'aromatiques.
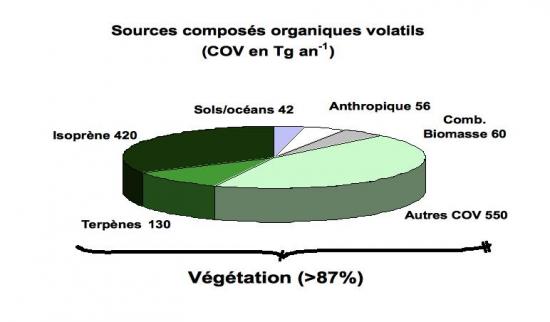
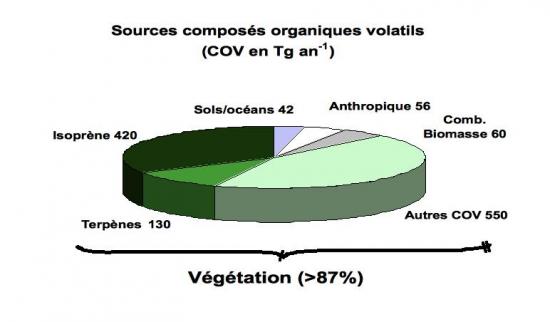
La végétation quant à elle, émet naturellement une grande diversité de COVs dans l'atmosphère (contribution > 87% figure 1). Ces composés sont caractérisés par une double liaison qui rend les molécules très réactives. Le principal composé émis est l’isoprène (C5H8, 2-méthyle-1,3-butadiène ou CH2C(CH3)CHCH2). L'isoprène est émis par un grand nombre d'espèces caduques, les composés terpénoïdes étant préférentiellement émis par les conifères. Ces émissions sont dépendantes de la lumière (rayonnement) et de la température.
La spéciation de la totalité des composés carbonés permet donc de déterminer en premier lieu l’influence des différentes sources sur la composition de l’atmosphère. Mais si l’on observe cette spéciation suffisamment en aval des sources de composés carbonés, leur abondance relative ne traduira pas uniquement celle des sources, mais aussi la réactivité du milieu atmosphérique vis à vis de ces différents composés.Des hydrocarbures d’origine anthropique comme propane, n-butane, isopentane, benzène et toluène sont transportés depuis les régions polluées.L’abondance relative mesurée du propane et de l’isopentane est cependant 5 fois plus faible que le rapport attendu pour tous ces composés émis en quantité équivalente par l’activité humaine. Ceci traduit la différence de réactivité de l’atmosphère vis-à-vis de ces deux composés.
II.2 Les composés organiques oxygénés
Les hydrocarbures oxygénés sont regroupés dans les différentes familles: aldéhydes (RCOH), cétones (RCOR), acides (RCOOH), et alcools (ROH)
Des composés organiques oxygénés résultent, comme pour le CO, à la fois de sources localisées à la surface, et de mécanismes de dégradation photochimique du méthane et des NMHCs. Ils sont présents en très grand nombre dans l’atmosphère. Les plus abondants de ces composés sont le méthanol (CH3OH) et l’acétone ((CH3)2CO). Ces deux espèces sont émises en grande quantité par la biosphère et sont aussi les moins réactives vis-à-vis du radical OH, avec des constantes de vitesse de l’oxydation par OH du même ordre de grandeur que pour le CO. Leur temps de vie* suffisamment long leur permet d'être transportées loin des sources : 100 jours pour l'acétone et 15 jours pour le méthanol (malgré une grande solubilité de ce constituant en phase aqueuse).
Parmi les composés très importants pour la chimie atmosphérique, on compte aussi le formaldéhyde (CH2O ou HCHO) et l’hydroperoxyde de méthyle (CH3OOH). La présence de ces composés loin des sources résulte principalement de l’existence d’une production in situ car leurs temps de vie ou temps de résidence dans l'atmosphère* (généralement inférieur à 1–2 jours) ne permettent pas un transport à longue distance. Ce temps de résidence* est principalement déterminé par la réaction avec OH qui est de 5–10 fois plus rapide que celle de CO, mais il faut aussi tenir compte de la photolyse.
CH2O et CH3OOH sont solubles dans l’eau et peuvent donc être éliminés du milieu atmosphérique par lessivage dans les nuages, limitant ainsi leur durée de vie. Même si ce temps de vie est court comparé à CH4 ou CO, il reste néanmoins suffisamment long pour permettre, comme dans le cas des NOx, un transport de ces deux espèces loin de leur zone de production où ils peuvent ensuite redonner des radicaux OH et HO2 par photolyse: CH2O et CH3OOH sont donc des espèces réservoirs*.
III Sources et puits de COVs
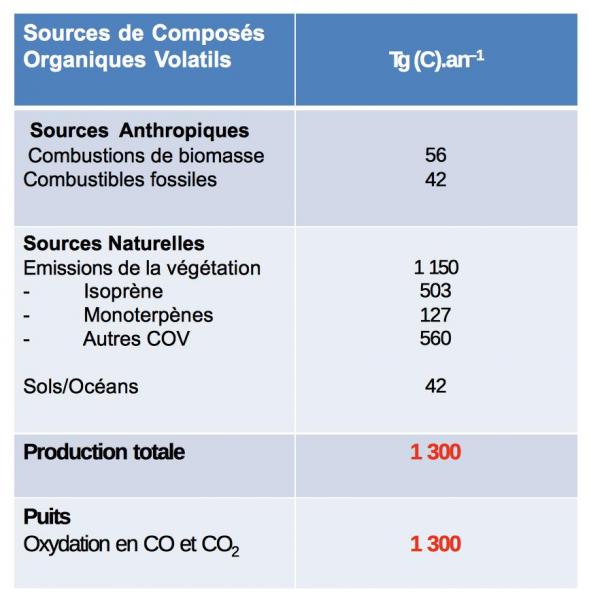
Le tableau 1 montre clairement que les sources majeures de composés organiques volatils sont constituées par la végétation naturelle qui représente plus de 87% du total des émissions. L’isoprène est le composé dominant émis suivi des monoterpènes, els autres composé émis sont principalement des hydrocarbures oxygénés. Ces émissions sont cependant des émissions diffuses. Les sources anthropiques sont environ dix fois plus faibles, mais les émissions sont beaucoup plus concentrées, notamment à proximité des industries, conduisant à la formation de panaches d’ozone dans lesquels la production est aussi stimulée par l’apport des hydrocarbures d’origine biogénique lors du transport des masses d’air.
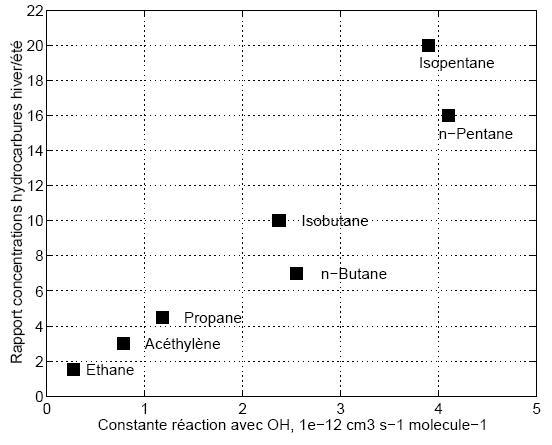
Comme pour le méthane (CH4), l’oxydation par le radical OH va être la principale cause de disparition de ces composés: la constante cinétique de cette réaction diffère fortement d'un hydrocarbure à l'autre. Une façon de mettre en évidence l’influence de la réactivité vis-à-vis de OH sur les concentrations d’hydrocarbures consiste à analyser dans un site éloigné des sources le rapport hiver/été des concentrations de différents hydrocarbures: les concentrations de OH étant beaucoup plus fortes en été, le rapport hiver/été doit être d’autant plus grand que la réactivité vis-à-vis de OH est grande. C'est ce que l'on observe dans les données collectées aux Iles Canaries (cf. Figure 2) où le rapport hiver/été de plusieurs hydrocarbures est effectivement corrélé linéairement avec la constante de réaction vis-à-vis de OH.
IV Les COVs dans l’atmosphère
Les COVs sont mobilisés dans des réactions photochimiques de la basse atmosphère, participant ainsi à l’augmentation de la concentration d’ozone dans la troposphère. Ils ont ainsi un effet indirect sur la santé et également sur le climat car l’ozone troposphérique et un des principaux gaz à effet de serre.
En bout de chaine d’oxydation les COVs oxygénés sont des acides organiques (formique (HCOOH), acétique (CH3COOH), propionique, butyrique….etc.) qui participent de façon significative à l’acidité des eaux de pluies en raison de leur forte solubilité.
Les COVs ont aussi un impact direct sur la santé, ainsi certains COVs peuvent provoquer des irritations sensorielles (hydrocarbures et formaldéhyde). Des manifestations plus sévères telles que les troubles cardiaques (toluène, chloroforme) et digestifs, ou les effets cancérogènes (benzène) et mutagènes, sont liés à des expositions chroniques ou intenses observées dans le passé dans certaines ambiances de travail. Les concentrations relevées dans l’environnement sont très inférieures à ces atmosphères et n’entraînent pas d’exposition aiguë.
Glossaire
Espèce réservoir: Une espèce réservoir est un composé chimique qui peut momentanément immobiliser sous une forme plus stable un composé réactif de l'atmosphère, par exemple un catalyseur. Les espèces réservoirs limitent d'autant plus l'efficacité de destruction d'un catalyseur que leurs stabilités et donc leurs efficacités de stockage sont grandes.
Temps de résidence dans l'atmosphère: le temps de résidence ou temps de séjour est la durée moyenne pendant laquelle une molécule d’un gaz donné ou une particule est présente dans l’atmosphère. Le temps de séjour des constituants mineurs dans l’atmosphère est conditionné par l’efficacité des puits (ou processus de disparition du réservoir atmosphérique). Ces puits sont essentiellement le dépôt à la surface et les réactions chimiques. Il existe des échanges permanents de matière entre les différentes sphères de l’environnement, lesquelles sont assimilées à des réservoirs. Les échanges comprennent les flux de matière entrant et sortant du réservoir et l’évolution interne du réservoir. La conservation de la matière impose une équation qui décrit l’évolution de la concentration au sein du réservoir en fonction du temps.
Le cas le plus simple est constitué par un réservoir de volume V où, à l’échelle de temps considérée, la quantité totale d’une espèce chimique Q présente n’évolue pas, et où la concentration C peut être considérée comme constante si l’on néglige les termes d’advection et de diffusion. On a alors :
Fe - Fs + S - P = 0
Alors les flux d’entrée représentant la somme des sources (Fe + S) et les flux de sortie représentant la somme des puits (Fs + P) sont égaux, et on peut définir un temps de résidence t de la matière au sein du réservoir (modèle de boîte).
Avec:
t = Q / (Fs+P) = (V*C) / (Fs+P)
Fs + P inclue le dépôt au sol et les transformations chimiques qui peuvent être complexes.
Cette définition permet de calculer le temps de résidence moyen d'une espèce chimique au sein du réservoir atmosphérique.
Par exemple, pour le méthane :
- masse totale de CH4 dans l'atmosphère : 4,3.1015 g ;
- somme des puits ~ 4,8.1014 g.an-1 ;
- temps de résidence moyen : τ = 9 ans.