Mécanismes
Cycle de l’azote
La disponibilité de l’azote contrôle de nombreux aspects de la biogéochimie globale. Elle limite souvent le taux de production de la biosphère, aussi bien sur les continents que dans l’océan.
Les réservoirs d’azote
Le principal réservoir d’azote est l’atmosphère avec 3,8.1021 g (N) sous forme d’azote moléculaire (N2), l’océan ne contenant que 2,2.1019 g (N) sous cette même forme (voir tableau). Le stock d’azote dans la biomasse terrestre est comparativement faible. L’azote y est présent essentiellement sous forme organique ou sous forme de nitrates et d’ammonium.
Les échanges d’azote dans l’environnement terrestre
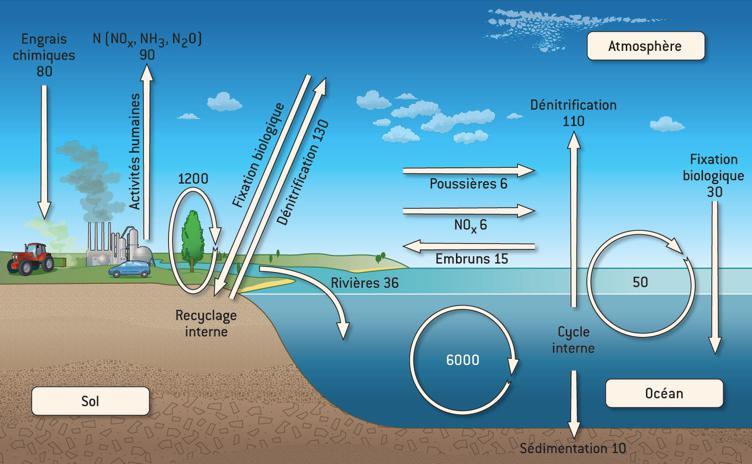
Que ce soit pour l’océan ou les continents, une partie essentielle du cycle de l’azote s’accomplit via des processus internes de minéralisation-réassimilation, car l’azote est utilisé (assimilé) par la biomasse essentiellement sous forme minérale. Ces ions proviennent de la minéralisation de la matière organique au cours de la décomposition bactérienne de la matière morte. Le cycle de l’azote est donc dominé par les transformations microbiennes, qui se différencient selon qu’elles interviennent en condition d’aérobiose (présence d’oxygène) ou d’anaérobiose (absence d’oxygène). Ces transformations font intervenir des groupes bactériens spécifiques
I Les réservoirs d’azote
La disponibilité de l’azote contrôle de nombreux aspects de la biogéochimie globale. Elle limite souvent le taux de production de la biosphère, aussi bien sur les continents que dans l’océan.
Le principal réservoir d’azote est l’atmosphère avec 3,8.1021 g (N) sous forme d’azote moléculaire (N2), l’océan ne contenant que 2,2.1019 g (N) sous cette même forme (voir tableau). Le stock d’azote dans la biomasse terrestre est comparativement faible. L’azote y est présent essentiellement sous forme organique ou sous forme de nitrates et d’ammonium.
| Réservoir | Espèce ou forme de l’azote | Stock en GT (1015g) |
| Atmosphère | N2 NOx, N2O NH3 | 3 800 000 1,4 0,0017 |
| Océan | N2 NO3 NH4+ AOD (Azote Organique dissout) AOP (Azote Organique particulaire) | 22 000 570 7 530 3,2 |
| Biomasse continentale | N organique sol N inorganique sol Plantes Humus Biomasse animale Biomasse microbienne | 300 160 11-14 1,9-3,3 0,17 0,5 |
Tableau 1. Principaux réservoirs et stocks d’azote dans l’environnement terrestre
II Les échanges d’azote dans l’environnement terrestre
Que ce soit pour l’océan ou les continents, une partie essentielle du cycle de l’azote s’accomplit viades processus internesde
-réassimilation, car l’azote est utilisé (assimilé) par la biomasse essentiellement sous forme minérale (NO3-,NH4+). Ces ions proviennent de la minéralisation de la matière organique au cours de la décomposition bactérienne de la matière morte. Le cycle de l’azote est donc dominé par les transformations microbiennes, qui se différencient selon qu’elles interviennent en condition d’aérobiose (présence d’oxygène) ou d’anaérobiose (absence d’oxygène). Ces transformations font intervenir des groupes bactériens spécifiques.
Les échanges avec l’atmosphère sont dominés par les échanges naturels d’azote moléculaire :
- de N2 par des bactéries spécifiques qui transforment N2 en NH4+ assimilable par la biosphère ;
- dénitrification : réduction des nitrates en N2O, puis N2 en conditions d’anaérobiose par d’autres groupes bactériens.
Une partie, limitée, des échanges intervient sous forme particulaire, à travers les aérosols marins ou terrigènes contenant des ions NO3- et NH4+.
La partie atmosphérique du cycle de l’azote ne peut cependant pas se réduire aux échanges d’azote moléculaire. En effet, au cours des transformations biologiques dans la biosphère, les processus bactériens font intervenir des intermédiaires gazeux, qui sont des composés azotés réactifs ayant un impact important sur la chimie de l’atmosphère :
- ammonification : formation de NH3 ;
- nitrification et dénitrification : formation de NO et de N2O ;
Une fraction significative des composés gazeux produits (NH3 et surtout NO et N2O) est libérée dans l’atmosphère au cours de ces processus. Le monoxyde d’azote est un des principaux précurseurs de l’ozone troposphérique. Son oxydation conduit par ailleurs à la formation d’acide nitrique (HNO3) qui participe à l’acidification des eaux de pluie. Le protoxyde d’azote (N2O), non réactif dans la troposphère, est
dans la stratosphère, où il intervient dans le
de formation/destruction de l’ozone. NH3 est essentiellement recyclé en phase liquide sous forme d’ion dans les précipitations.
Les perturbations anthropiques du cycle de l’azote sont de deux ordres :
- émission d’oxydes d’azote par les combustions de combustibles fossiles et de la biomasse (30 à 40 MT(N).an–1) ;
- l’utilisation des engrais chimiques, produits par fixation d’azote atmosphérique (80 MT(N).an–1). Cet azote sert principalement à stimuler la production primaire (cultures). Toutefois, une fraction significative est restituée à l’atmosphère sous forme de composés réactifs, en particulier le monoxyde d'azote NO.